A termodinâmica é uma área da física que se concentra em estudar as transferências de energia através das relações entre calor, energia e trabalho. Essa observação se dá pela análise de fenômenos em que há trocas de quantidade de calor, bem como troca no trabalho empregado em um processo físico.
Essa área da física, caracterizada como termodinâmica, foi desenvolvida por pesquisadores, ainda na revolução industrial, que buscavam maneiras de aprimoramento mecânico das máquinas. Em resumo, para a conjuntura da época, um bom desempenho das máquinas era primordial para a consolidação da grande mudança que a mecanização significa até hoje.
Contudo, quando levamos em consideração que todos os aparelhos presentes em nosso cotidiano, percebemos como este fenômeno está mais presente do que nunca, por exemplo, em máquinas térmicas e refrigeradores. Sobretudo, esse fenômeno está presente na cozinha.
Enfim, as leis fundamentais da termodinâmica apresentam a relação de como o calor vira trabalho e vice-versa. Ou seja, como a energia é gerada ou utilizada em um dado sistema.

Conceitos fundamentais
- Calor : é a troca de energia térmica entre corpos, ou seja, é a energia empregada que um corpo deposita em outro;
- Energia: se refere a quantidade de trabalho empregado por um corpo para realizar um movimento;
- Temperatura: diz respeito a agitação das moléculas. Como resultado disso, quanto mais calor, mais agitadas; quanto menos calor, menos agitadas;
- Volume: diz respeito ao espaço ocupado pelas moléculas em análise;
- Pressão: a pressão é o resultado do movimento das partículas em um recipiente.
1ª lei da termodinâmica

Primeiramente, essa primeira lei se baseia no princípio da conservação de energia. Ou seja, a energia que está presente em um sistema não pode ser destruída e nem criada. Essa energia apenas se transforma por meio de trabalho empregado nesse sistema e quantidade de calor. Sua equação é:
2ª lei da termodinâmica
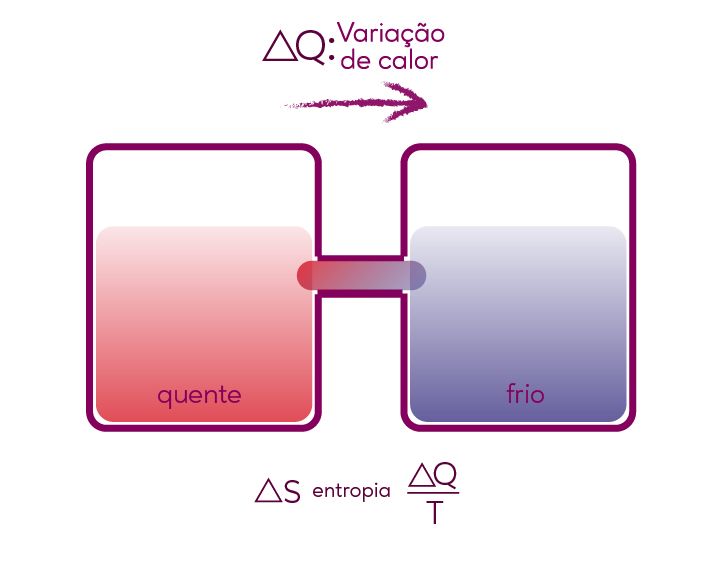
Já essa lei se baseia na observação da transferência de calor espontaneamente. Também conhecida como entropia, essa transferência de calor ocorre sempre do corpo mais quente para o corpo mais frio, sendo este processo, irreversível. O calor não é passível de se converter integralmente em outra, porque é uma forma degradada de energia. Quando empregada, dissipa-se.
Lei zero
Essa lei é chamada de lei zero porque é basilar para as outras duas leis anteriores. Essa lei baseia a condição para obter uma forma de equilíbrio térmico. Conforme a 1ª lei, o calor que é empregado, só pode se transformar, ou seja, se degradar; já que, como consta na 2ª lei, a transferência de calor é irreversível.
Dois corpos em temperaturas diferentes, quando em contato, passa a predominar a temperatura do mais quente, que se dissipa para o mais frio até que as temperaturas se igualem, alcançando o equilíbrio térmico como resultado disso.
3ª lei da termodinâmica
Essa lei é motivo de polêmica para alguns pesquisadores, já que, apesar de ser chamada de lei, mais se assemelha à uma regra. A 3ª lei da termodinâmica é uma maneira de tentar estabelecer um ponto absoluto de referência como marco para a entropia; ou seja, um ponto de referência para o grau de desordem de um sistema, calculado pela 2ª lei da termodinâmica.
A partir de um limite inferior de temperatura (zero absoluto), esta lei diz que não é possível que uma substância alcance a temperatura do zero absoluto. É a partir dessa perspectiva que se é possível verificar implicações acerca do rendimento de máquinas térmicas que jamais alcançaram a posição de rendimento igual à 100%.
Sistema termodinâmico
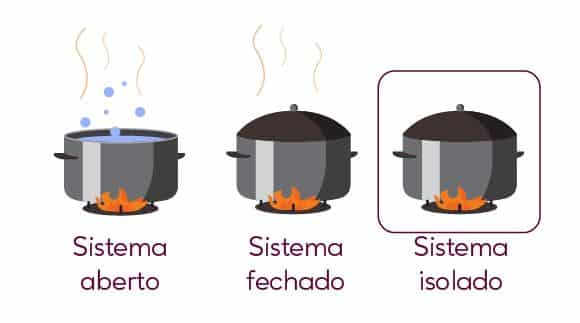
O sistema, na termodinâmica, diz respeito ao espaço em que um ou mais corpos se relacionam com o ‘meio’ ou o ‘universo’ externo a esse sistema, podendo ser fechado, aberto ou isolado. Se aberto, há troca de calor e massa com o meio; já o fechado, há troca de calor apenas. E o isolado, não há trocas de calor e nem de massa.
Estado térmico
O estado térmico diz respeito ao comportamento das moléculas; estas que são avaliadas por moléculas de gases chamados de gases ideais. O estado térmico é mais facilmente avaliado nos gases do que em outros estados físicos, tais como o líquido e o sólido.
Os gases ideais são cenários em que as moléculas se movem caoticamente e só interagem em suas colisões, sendo essas colisões consideradas ‘elásticas’, por durarem pouco tempo. Essa avaliação já coloca em cena outras grandezas: pressão, volume e temperatura.
A Termodinâmica no cotidiano
Agora que você já saber como funciona a teoria da termodinâmica, que tal (re)conhecer algumas hábitos do dia-a-dia que são a pura pratica de todas essas teorias?!
A temida temperagem do chocolate
Conhecida também como Banho Maria, essa troca de temperaturas gradativa é a prática da 2ª da termodinâmica.

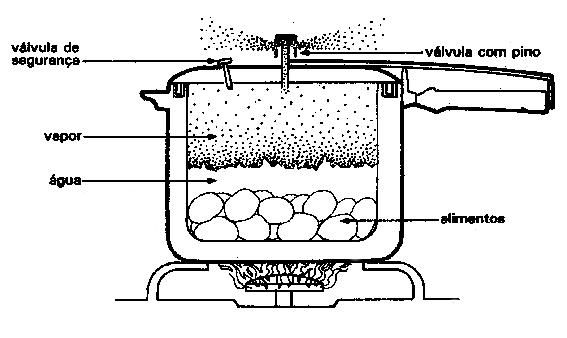
A panela de pressão
A panela de pressão diminui a saída de temperatura e de massa, fazendo com que a pressão aumente com a agitação das moléculas, oriundas da temperatura empregada com o fogo do fogão.
A garrafa térmica
Seu nome original é ‘vaso de Dewar’, mas popularmente ficou conhecido como Garrafa Térmica. É composto por um recipiente que consegue ter um isolamento térmico praticamente perfeito. Como resultado disso, consegue ter uma capacidade de conserva térmica prolongada porque evita a troca de calor com o meio exterior.

Por fim, você gostou dessa matéria? Então você também vai gostar dessa: Panela de pressão – Com funciona, como usar, cuidados e receitas
Imagens: Sabores Ajinomoto. Unsplash, socorro na cozinha.
Fontess: Descomplica, Toda materia, Brasil Escola, Prepara Enem.



foi mal dei uma estrela sem quere 🙁